논문정보
Deep Learning-Based Automated Quantification of Coronary Artery Calcification
for Contrast-Enhanced Coronary Computed Tomographic Angiography
논문정리
Abstract
<Background>
향상된 ECG-gated CCTA(coronary CT angiography)를 기반으로 한
딥러닝 기반 자동 정량화 알고리즘의 관상동맥 석회화 (CAC, coronary artery calcium) 측정 정확도를 CT(CSCT)로 평가함
즉, 딥러닝이 석회화를 얼마나 정확하게 잘 뽑는지를 확인
CSCT
조영제 없이 촬영해서 관상동맥에 칼슘(석회화)이 얼마나 쌓였는지 점수화하는 CT
심혈관 질환 위험 예측에 사용됨
* 왜 CSCT는 조영제를 안쓸까,,?
CSCT, Coronary Calcium Scoring CT는 혈관에 칼슘이 얼마나 있는지를 보는 검사!
조영제는 혈관이나 장기 내부에 혈액이 흐르는 모양을 뚜렷하게 보기 위한 용도
▶️ 혈관의 루멘을 확인할 때 필요!
CSCT는 혈관벽에 박힌 칼슘만 보고자 해서 칼슘처럼 X선을 잘 막는(=고밀도) 물질의 위치를 찾음
따라서, 조영제 없이도 충분히 보임!!!
why? 칼슘은 밀도가 높아서 조영제 없이도 CT에서 밝게 찍히니까!
<Methods>
같은 날 CSCT와 CCTA를 시행한 315명의 환자로 연구
- 200명은 내부 검증 세트 (본적 있는 데이터)
- 115명은 외부 검증 세트 (처음 보는 데이터)
CCTA의 자동화 알고리즘과 CSCT의 기존 방법을 통해 칼슘 용적(volume)과 Agatston score + 계산 소요 시간 평가
본 알고리즘은 평균적으로 5분 이내에 관상동맥 석회화를 추출했으며, 이때 실패율은 1.3%
모델이 계산한 칼슘 용적과 Agatston 점수는 CSCT 결과와 비교했을때, 일치 상관계수는 내부셋에서 0.90~0.97, 외부에서 0.76~0.94로 높은 상관계수를 보임
분류 정확도는 내부에서 95%(0.94 weighted kappa), 외부에서 86%(0.91 weighted kappa)를 보임
Weighted kappa
두 분류 결과가 얼마나 비슷한지를 수치화
딥러닝 기반의 자동화 알고리즘은 추가적인 방사선 노출 없이도 CCTA에서 관상동맥 석회화를 효율적으로 추출하고, Agatston 점수에 따른 등급 분류도 안정적으로 수행
1. Introduction
CAC(coronary artery calcium)의 양은 심혈관 질환 발생을 예측하는 매우 강력한 지표
CAC가 많을 수록 심근경색, 협심증 같은 심혈관사건 발생 확률이 높아짐
▶️ CAC를 정량화하기 위한 다양한 방법들이 시도되었음
- 기준(reference)로 활용되는 전용 CSCT
- 관전압을 낮추거나 iterative reconstruction, high-pitch 스캔 등을 사용해 방사선을 줄인 CSCT
- ECG(심장 신호) 없이 찍은 일반 흉부 CT를 이용
- 조영제를 사용하고 ECG 신호에 맞춰 촬영한 관상동맥 CT(CCTA)에서 CAC를 추출
그 중, CCTA를 활용한 CAC 추출 방법이 전용 CSCT 촬영을 생략해도 되서 방사선 노출을 줄일 수 있다는 장점
여러 연구에서 조영제를 사용한 CCTA를 기반으로 CAC를 정량화하는 자동화 시스템의 유용성을 입증함
but, 실패율이 7~8%로 높고 관전압(tube voltage)이나 CT 장비의 다양성이 부족하다는 제한점이 있음
특정 조건 (장비, 설정)에만 작동해서 일반 병원 적용 어려움
칼슘 추출을 위한 adaptived threshold 기법과 Agatston 점수 계산을 위한 weight-decision 기법을 활용한, 완전 자동 딥러닝 기반의 새로운 접근 방식이 한계를 극복하고 다양한 관전압 조건의 CCTA 스캔에서도 높은 안정성을 보일것이라 예상함
adaptive threshold ▶️ 상황에 따라 칼슘 경계값을 자동으로 조절
다양한 kilovoltage peaks▶️ 현실적인 조건 반영하려는 시도
Tube Voltage (관전압)
CT나 X-ray에서 X선을 발생시킬때 사용하는 전압
단위는 킬로볼트 피크 (kVp, kilovolt peak)
따라서 이 연구는 조영제 사용 및 ECG-gated CCTA를 기반으로 한 딥러닝 기반 자동 정량화 알고리즘의 정확도를, CSCT를 reference로 하여 비교평가 하는것이 목적!
2. Materials and Methods
2.1 Data Collection
같은 날 CSCT와 CCTA 검사를 받은 총 315명을 대상
- 건강검진센터에서 검사를 받은 200명의 internal validation group
- 서울대병원에서 동일한 검사를 받은 115명의 external validation group
Internal validation group은 건강검진 목적으로 자발적 검사를 받은 사람들이고, external validation group은 관상동맥질환 평가를 위해 병원에서 진료 목적으로 심장 CT를 받은 사람들임
두 그룹의 성격이 다른데, 내부그룹은 그냥 건강검진 받으러 온 사람들이라 보통은 증상이 없는 경우가 많음
반면, 외부 그룹은 실제로 의심 증상이 있어서 병원에서 검사받은 사람들
제외 기준
- 20세 미만 (관상동맥 질환 위험이 거의 없는 연령)
- 금속 스텐트 삽입 (금속 인공물 때문에 칼슘을 제대로 구분하기 힘듦)
- 관상동맥 우회수술(CABG) 이력
2.2 CT Image Acquisition
건강검진센터에서는 2세대 dual-source CT 스캐너 (Somatom definition flash),
서울대 병원에서는 1세대 (Somatom Definition)or 3세대 (somatom Force) 사용
촬영 전 심박수가 70bpm 이상인 환자는 beta-blocker 금기사항이 없는 경우 CT촬영 30~60분 전에 metapropol 100mg 경구투입
심장이 빠르게 뛰면 CT영상이 흔들려서 흐릿해질 수 있기 때문에
심박수를 안정시키기 위해, 메토프로폴(심장박동을 느리게 하는 약)을 미리 복용시킴
CSCT는 심전도(ECG) 신호에 기반한 prospective 트리거 방식을 아용해서 R-R 간격의 70% 시점에 촬영되었으며, 관전압 120 kVp, 관전류시간 60 mAs, 단층 두께 3mm, 간격 3mm, 재구성 기법은 필터 역투영을 사용
심장 박동 사이에서 가장 정지에 가까운 순간 (70%)을 골라 촬영하면 흔들림 없이 칼슘을 정확히 볼 수 있음
금기사항이 없는 경우, 체중이 60kg 이상인 환자에게는 0.4mg, 미만이면 0.2mg의 sublingual nitroglycerin을 투여한 후 CCTA 영상 획득
니트로글리세린은 혈관을 넓혀주는 약
60~80ml의 nonionic 조영제를 45ml/s 속도로 이중 전동 주입기로 주입
영상 획득 타이밍은 상승 대동맥 중간 부위에 ROI(region of interest)를 지정한 bolus tracking 기법으로 결정
trigger threshold, delay는 100HU에서 15초, FLASH 모드는 150HU에서 8초 후에 촬영
관전압(tube voltage)와 관전류(tube current)는 자동 관전압 선택 소프트웨어(CARE kV)와 자동 노출 조절 시스템(Care Dose 4D)을 기반으로 개별 설정
CCTA 영상 재구성에 사용된 세부 파라미터는 단층 두께 0.75mm, 재구성 간격 0.4~0.5mm
내부 병원에서는 I26f 커널과 SAFIRE(강도 3), 외부 병원에서는 Bv40 커널과 ADMIRE(강도 3)의 반복 재구성 기법을 사용
1세대 dual-source CT는 interative reconstruction을 수행하지 않음
Iterative reconstruction
반복 계산을 통해 노이즈를 줄이고 해상도를 높이는 영상 복원 방식
2.3 Reference Calcium Scores
CAC를 정량화하기 위해 Volume score, Agatston score 사용
부피가 얼마나 큰가? (volume) & 얼마나 심한가? ( Agatston )
1mm² 이상의 면적을 가지면서 CT 감쇠값(peak attenuations)이 130HU르 초과하는 연속 픽셀들을 석회화로 간주하여 정량화함
즉, Volume score는 석회화의 부피(mm³)를, Agatston 점수는 병변의 면적에 그 병변 최대 감쇠값을 가중치로 곱해 계산
작아도 매우 밀도가 높은 칼슘은 위험할 수 있으니 가중치를 높게 준다
최대 감쇠값에 따른 가중치는
- 130~199HU: 1
- 200~299HU: 2
- 300~399HU: 3
- over 400HU: 4
모든 CSCT 영상은 워크스테이션(syngo CT Workspace)로 전송되었으며, 임상적으로 검증된 반자동 소프트웨어(syngo Calcium Scoring)를 통해 숙련된 방사선 기술자가 분석
2.4 Matrix Factorization Method
관상동맥 칼슘의 자동 세그멘테이션 및 정량화는 전용 심장 프로토타입 소프트웨어(AutuSeg-H ver.1.1.005)를 사용해 수행
+ 알고리즘을 사용항 칼슘 점수를 계산하는데 걸린 시간도 기록
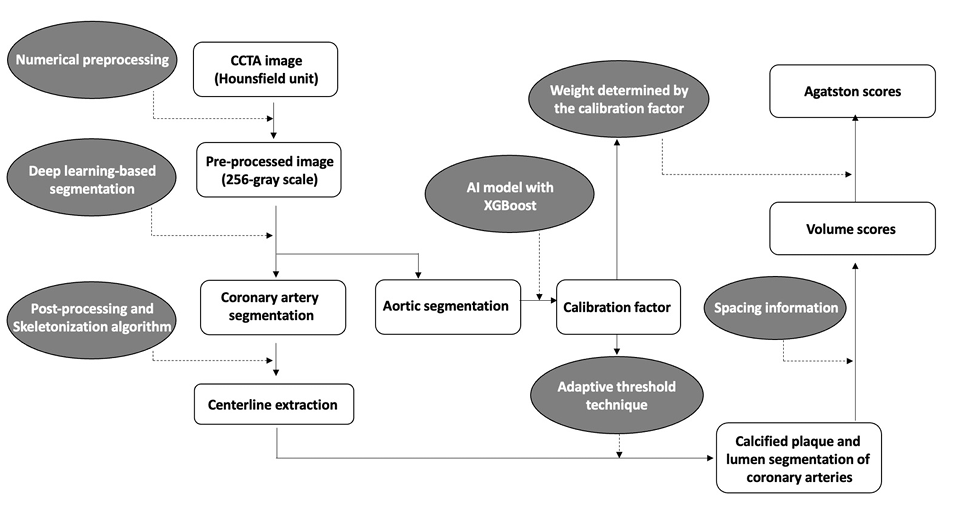
먼저 관상동맥을 선명하게 하고 세그멘테이션을 쉽게 하기 위해 contrast(조영제)-enhanced CCTA 영상을 여러 수치기법으로 전처리함
- 가우시안 혼합모델 기반의 expectation-maximization algorithm
- 새롭게 개발된 attenuation histogram optimization algorithm
- Hessian filter 적용
전처리된 영상을 v-net 기반의 2차원 딥러닝 네트워크가 2.5차원 방식으로 학습되어 관상동맥을 분할함
2.5D
2D 영상 슬라이스를 연속적으로 보면서 3D 처럼 파악하는 방식
Deeplab v3+은 calibration factor를 얻기 위해 상행 대동맥을 세그멘테이션
세그멘테이션된 상행 대동맥의 attenuation value로부터 XGBoost AI 기법으로 도출
이 인자는 (그림 2에서) 녹색으로 표시된 대동맥 부분의 단순평균 attentional value가 아님
근까 각 tube voltage 상황에서 단순 평균때린 값이 아니라 AI로 다양한 요소를 반영했다는거같음
그래서 여러 tube voltage에 specific하지 않게 칼슘을 추출할 수 있다

(a) 3D 모델
관상동맥 트리와 대동맥 세그멘테이션 결과
녹색 : 상행 대동맥 (ascending aorta), calibration factor를 계산하는데 쓰임
분홍색: 관상동맥(coronary arteries), 딥러닝 모델이 자동으로 혈관 구조를 세그멘테이션한 결과
(b) CSCT 영상에서의 석회화(칼슘) 영역
조영제가 없어서 밝게 보이는 부분 = 석회화된 부분(칼슘)
이 이미지는 딥러닝이 분석하는것이 아니라, reference 역할을 함
(c) CCTA 영상에서의 동일 위치
동일한 환자의 같은 부위를 조영제를 넣은 CT(CCTA)로 찍은 영상
(d) Segmentation 결과
칼슘의 위치를 녹색으로 세그멘테이션
대신 XGBoost 기법은 입력값으로 사용된 대동맥 부위(녹색으로 표현)의 attenuation value를 바탕으로 관상동맥의 대표 attenuation value를 추출하는데 사용
대동맥의 밝기를 참고해서 관상동맥의 밝기(=칼슘 판단 기준)를 보정하는 과정
▶️촬영 조건마다 달라지는 HU 기준점을 환자 맞춤형으로 계산
coronary tree의 세그멘테이션 결과에서 누락되거나 잘못 분류된 복셀(voxel)을 수정하기 위해 수치적 후처리 방법 적용
불연속적인 혈관을 연결하기 위해 관상동맥 구조와 위치, 거리, 유형 정보 사용
관상동맥으로 잘못 분류된 정맥이나 심장 조직 등의 복셀은 각도, 위치, 감쇠도 정보를 조합해 제거
후처리된 결과로부터 skeletonization algorithm을 통해 중심선(centerline)을 추출
이후, 계산된 calibration factor와 centerline의 각 단면 픽셀 정보를 이용한 adaptive treshold 기법을 통해 관상동맥의 루멘과 석회화 플라크 경계를 결정 (그림2)
Calibration factor는 관상동맥 centerline에서 얻어진 감쇠도 값의 부정확성을 보정하기 위한 역할을 함
⚠️헷갈리는 부분!
calibration factor = 기준값
adaptive threshold = 이 기준값을 활용해 계산된 판단 기준
Centerline에 칼슘이 존재해 관상동맥 감쇠도가 증가한 경우, 칼슘 검출 기준은 관상동맥 감쇠도가 아닌 보정 인자를 기반으로 정함
▶️ 픽셀의 감쇠도가 보정 인자의 1.45배를 초과하면 칼슘으로 인식
but, centerline을 통해 얻어진 관상동맥 감쇠도가 정확한 경우 ▶️ 픽셀 감쇠도가 관상동맥 centerline 감쇠도보다 1.25배 이상일 때 칼슘으로 판단
세그멘테이션 결과를 바탕으로 각 관상동맥 혈관에 대한 석회화 부피(calcification volume)가 spacing 정보를 이용해 추출됨
Agston 점수를 계산하기 위해 각 석회화 복셀의 감쇠도(HU)에 따른 adaptive weight 합산
HU가 높을수록 더 높은 가중치를 부여함
Adaptive weight는 calibration factor에 의해 결정되었는데, 이 tube votlage에 따른 calibration factor는 석회화 감쇠도의 변동성을 반영
같은 칼슘이라도 CT 관전압(kVp)이 달라지면 HU 값이 달라져서, 이걸 보정하려고 사용하는 기준값
Adaptive threshold 기법과 weight decision 방식은 CSCT에서 얻은 volume score 및 Agatston 점수를 기준으로 202개의 추가 케이스를 통해 조정함
관상동맥 세그멘테이션부터 석회화 정량화까지 한 케이스당 5분 소요
AMD RYZEN 5 560X와 RTX 3060GPU가 장착된 일반 개인용 컴퓨터에서 수행
2.5 Statistical Analysis
연속형변수(continuous variable)는 평균 ± 표준편차, 범주형변수(categorical variable)는 빈도와 백분율로 표현
연속형 변수 간 비교는 paired t-test를 사용
상관관계는 피어슨 상관계수로 분석
CAC 점수 간 일치도는 일치 상관계수 (CCCs)와 Bland-Altman plot을 통해 평가
Agatston 점수의 범주형 일치도는 weighted kappa 값으로 평가
Agatston 점수는 보통 위험군(1~5등급)으로 나눠서 평가
그 카테고리간 일치를 보는데 weighted kappa를 사용
kappa 값과 CCC 값에 따라 inter-method 일치도(agreement)는 다음과 같이 평가
- poor: 0.2이하
- fair: 0.21~0.4
- moderate: 0.41~0.6
- good: 0.61~0.80
- excellent: 0.81~1.00
자동 CAC 정량화(auto-CAC)의 다섯가지 범주형 위험 분류 정확도 분석
p-value가 0.05미만일때 통계적으로 유의한 것으로 간주
3. Results
3.1 Dataset Characteristics
표1에 내부 검증 그룹(n=200)과 외부 검증 그룹(n=115)의 기본 인구통계학적 특성 표기

검증 그룹 대상 수 주요 사용 관전압 (kVp)
관전압(kVp)는 CT 촬영의 핵심 파라미터로, 높을수록 방사선 세기가 강하고 HU값도 달라짐
| 내부 | 100 kVp (138명, 69%) | 80 kVp (49명, 24.5%) | 120 kVp (13명, 6.5%) | — |
| 외부 | 100 kVp (85명, 73.9%) | 80 kVp (24명, 20.9%) | 120 kVp (4명, 3.5%) | 90 kVp (2명, 1.7%) |
2.1 Performance of Automated Quantification of Coronary Calcium on Contrast-Enhanced CCTA
자동 알고리즘의 성능 평가는 실패 케이스를 제외하고 수행
전체 실패율은 1.3% (315건 중 4건)로, 내부 검증그룹과 외부 검증그룹에서 각각 2번씩 일어남
주 원인은 호흡에 의한 움직임 아티팩트와 부적절한 피치 설정
자동시스템으로 CAC 점수를 계산하는데 걸린 평균 시간은 5분 미만(292초), 표준편차는 18.8초
표 2에는 내부/외부 검증셋에서 해부학적 위치(anatomical location)별로 CSCT와 auto-CAC가 계산한 volume, Agatston socore의 평균값, 상관/일치계수 요약
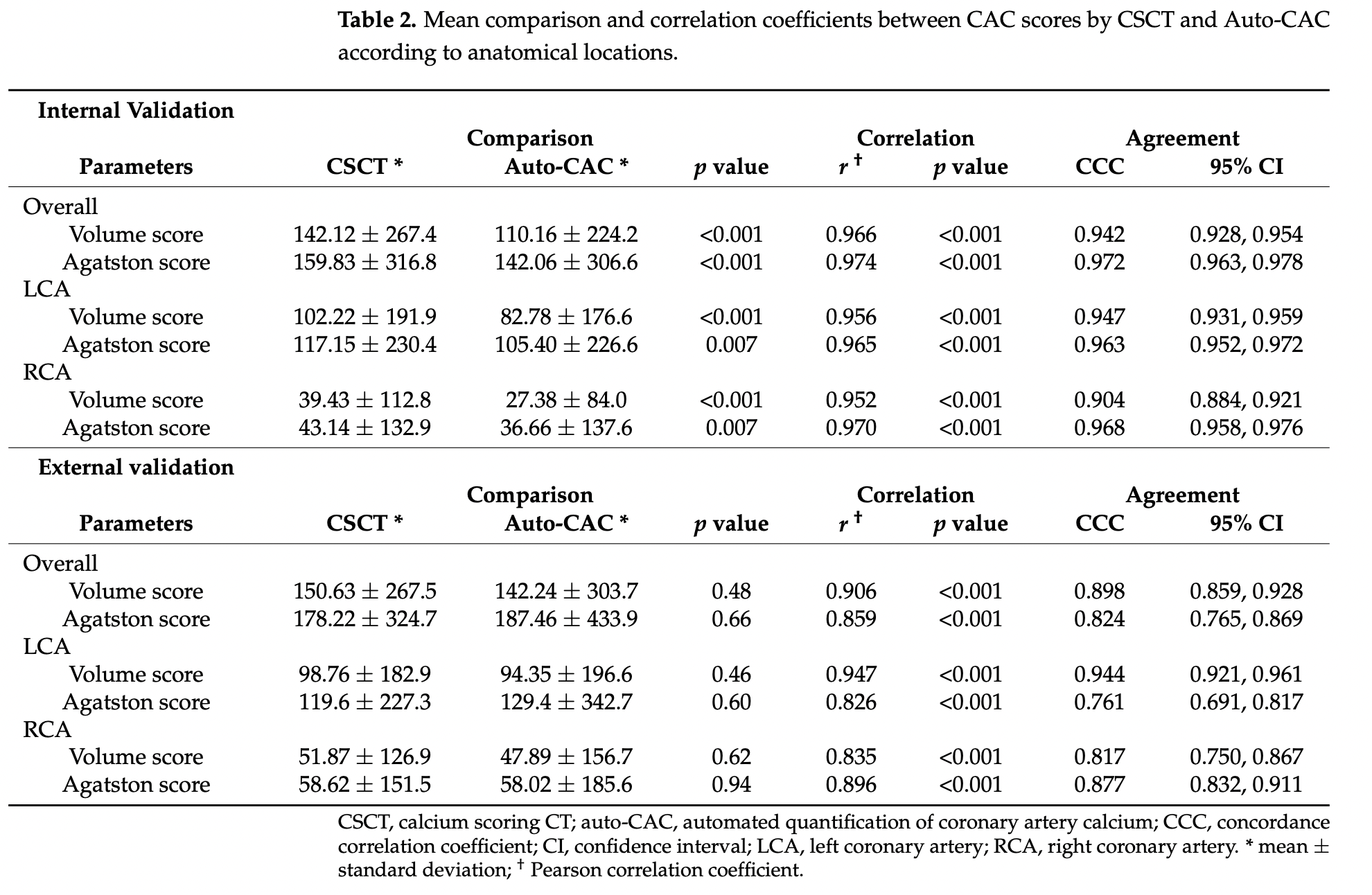
내부 검증셋에서는 auto-CAC, CSCT 사이의 평균 점수 간 유의한 차이가 있었지만, 외부 검증셋에서는 아녔음 (p>0.05)
외부병원 데이터에서 더 안정적으로 작동했다는..?
내부셋에서 volume, Agatston 점수의 평균 차이는 각각 -32.0, -17.8이고, 외부셋은 -8.4, -9.2
CSCT, auto-CAC간의 상관관계는 volume, Agatston 점수에서 모두 우수했음 ==> 그림 3
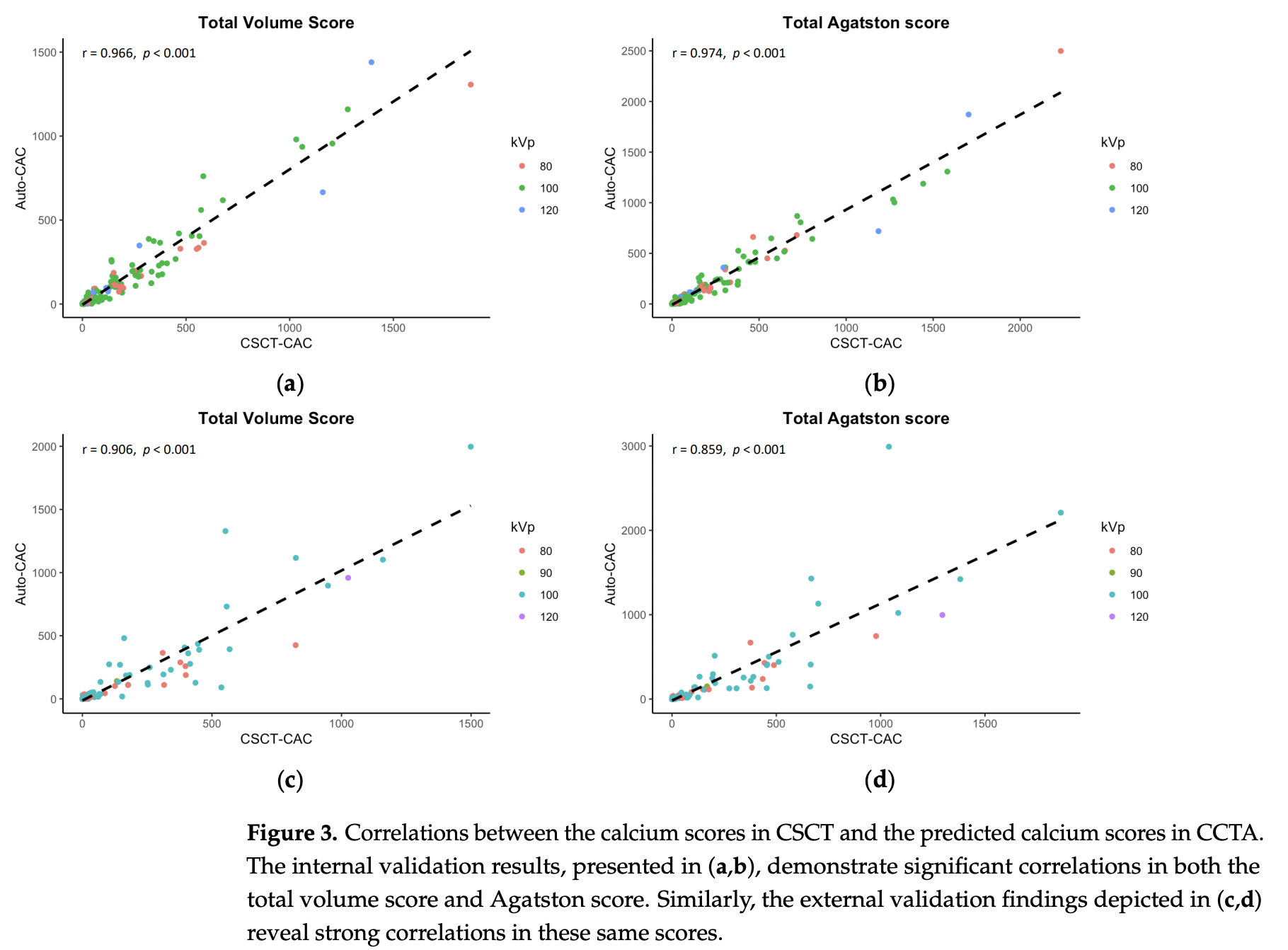
일치 상관계수 (CCC, concordance coreelation coefficients)도 내부/외부 검증셋의 모든 해부학적 위치에서 우수함

표3에서는 CSCT, auto-CAC 평균 점수값에 특히 volume score에서 유의한 차이가 일부 있었지만
표3과 그림3에서 볼 수 있듯, 내부/외부 검증셋에서 모두 volume, Agatston score에서 매우 우수한 상관관계가 관찰되었다.
모든 kVp 그룹에서도 두 검사의 일치도 우수
kVp가 바뀌면 HU값이 달라지지만, 보정인자 덕분에 정확도가 잘 유지되었음을 의미함
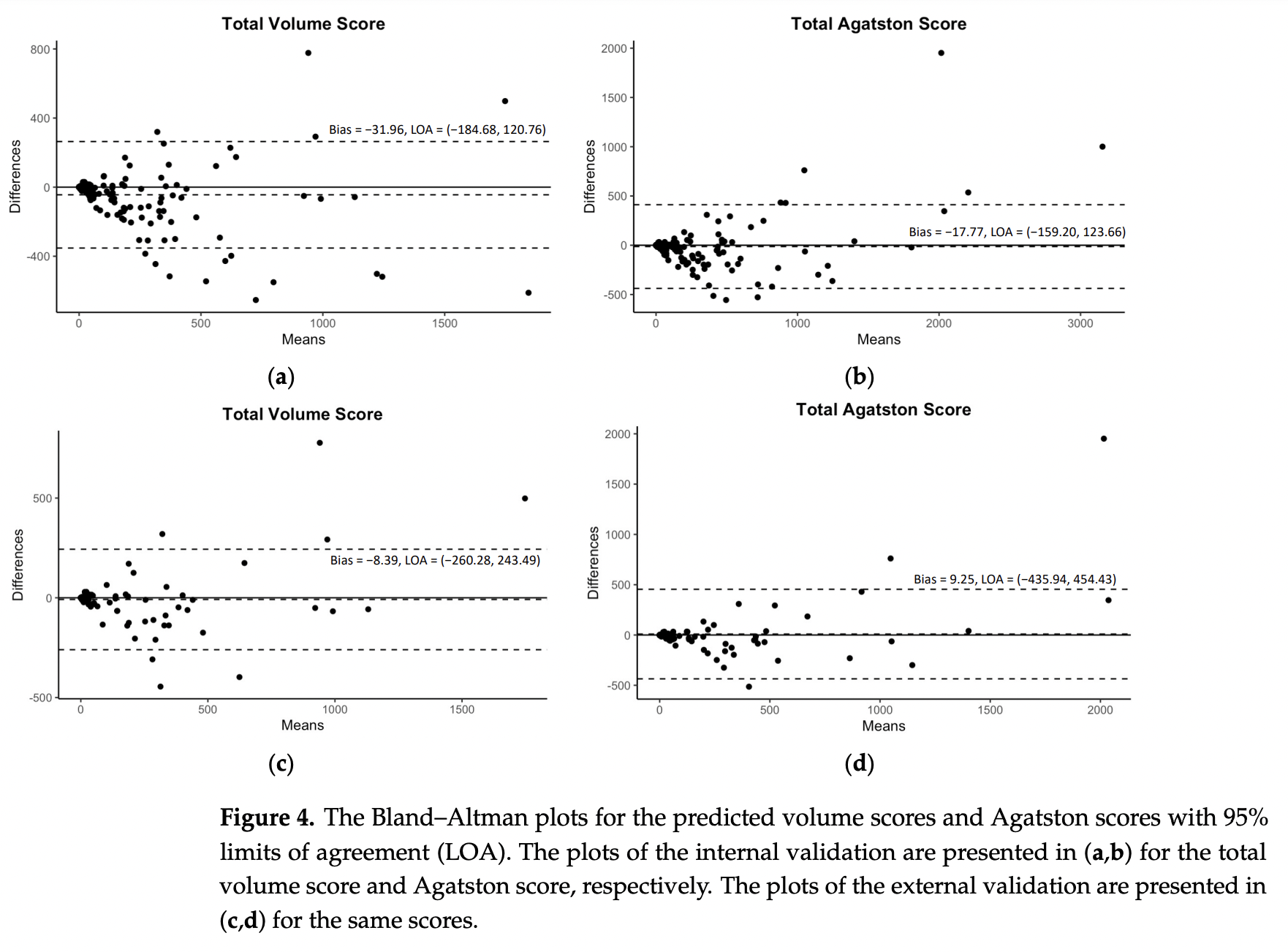
그림 4의 Bland-Altman plot에서는 CSCT, auto-CAC간의 차이에 뚜렷한 패턴이 없었고, 대부분이 점들이 95%ㅍ 신뢰구간 내에 위치했다.
두 점수간 차이가 한쪽으로 치우치지 않고 무작위로 분포하며, 대부분이 허용 오차 범위 내에 있다?
▶ 일관된 측정 성능!!
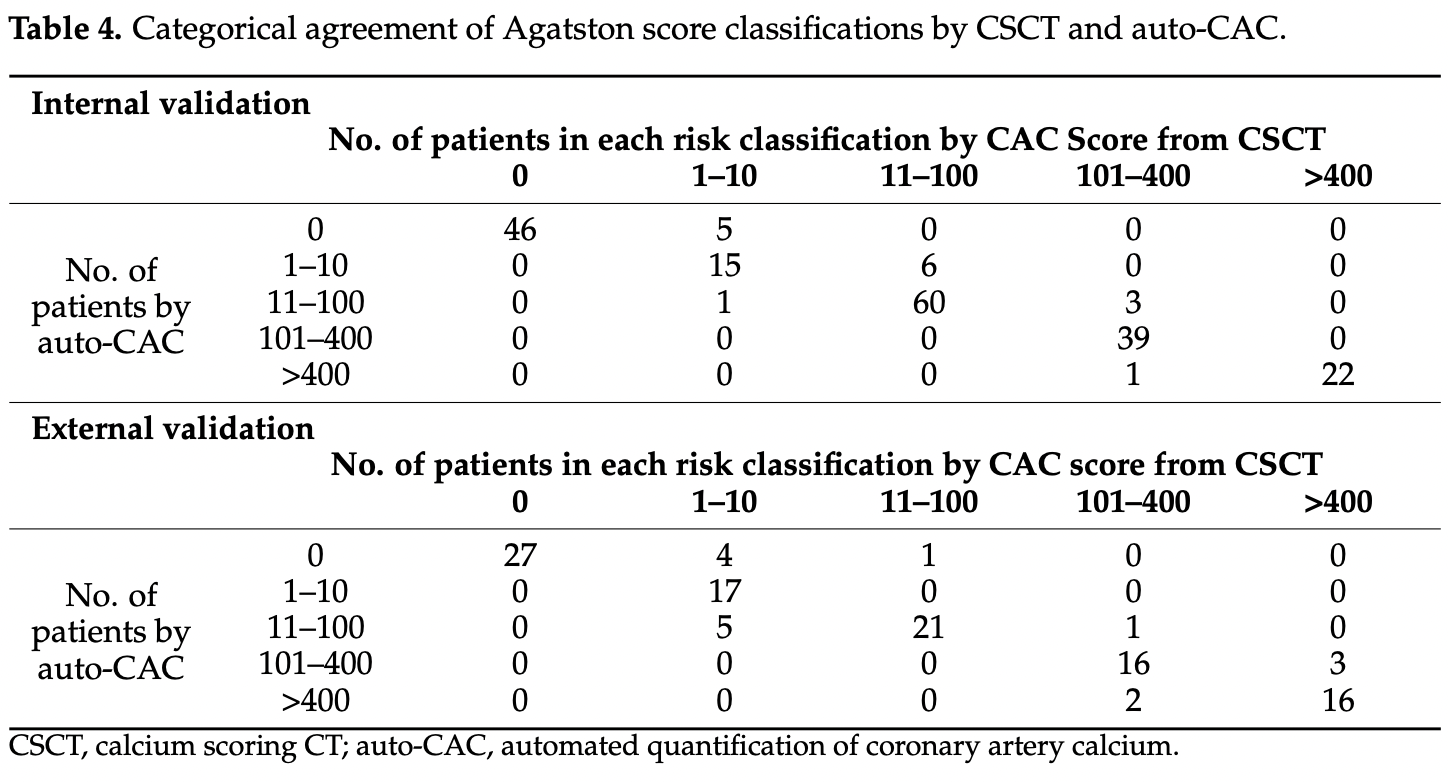
표 4에서 Agatston score의 범주형 위험도 분류 일치도는 내부와 외부 검증 모두에서 우수했다.
수치를 정확히 맞추는 것도 중요하지만, 실제로 환자를 위험군으로 분류하는게 임상에 더 중요함
내부 검증셋에서 위험도 분류 정확도는 91.9%, weighted kappa값은 0.945
내부 검증 세트에서 16명(8.1%)이 다른 실혈관 위험군으로 재분류되었고, 이 중 대부분(14명, 87.5%)은 더 낮은 위험군으로 분류되었다.
딥러닝이 조금 더 보수적으로 판단하는 경향이 있음, 과소평가
내부 검증 세트에서 100 kVp와 80 kVp의 분류 정확도는 각각 90.5%, 95.8%
외부검증 셋에서 16명(14.2%)이 다른 위험군으로 재분류되었고, 그 중 9명(56.2%)는 더 낮은 위험군으로 이동
외부 검증 세트에서 100 kVp와 80 kVp의 정확도는 각각 88.2%, 78.3%
4. Discussion
본 연구의 주요 결과, 딥러닝 기반 자동홤 델은
- CCTA로부터 CAC volume, Agatston score를 5분 이내, 실패율 1.3%로 효율적으로 추출
- CSCT 기준값과 매우 우수한 상관도와 일치도
- kVp와 무관하게 안정적인 성능
- 외부 검증에서 5단계 위험군 분류 정확도는 86%
기존 여러 연구에서도 contrast-enhanced CCTA 기반 CAC 정량화를 시도했고, 자동 모델로 추출한 CAC점수와 기준값 간의 피어슨 상관계수는 0.91~0.96으로 높은 상관관계를 기록
완전 자동화된 CAC 정량화 모델을 사용한 기존 연구들 중 외부 데이터셋에서 검증이 수행된 경우는 단 1개 뿐이며, 본 모델은 정확도 86%, weighted kappa 값 0.906으로 기존 연구들의 정확도 (67~84%) 및 weighted kappa 값 (0.78~0.906)보다 더 우수한 성능을 보임
모델의 높은 정확도와 적응성은, 석회화를 식별할 때, 상행 대동맥(ascending aorta)의 감쇠도를 활용한 적응한 임게값 방식 덕분
관상동맥 세그멘테이션 단계에서는 기존 수치 기반 방법(5~6%)보다 낮은 실패율 (1.25%)를 보였으며, 이는 딥러닝 기반 세그멘테이션의 안정성 덕분
CSCT로 얻은 CAC의 양은 무증상 환자의 심혈관 사건을 예측하는데 있어 유의한 예측 인자지만,증상 있는 환자에게는 그 임상적 의의가 제한적임
CSCT만으로는 한계가 있기에 CCTA를 활용하고자 하는 동기를 주는 듯
그치만 타연구에서는 CSCT의 CAC 점수와 CCTA 협착 정도를 함께 사용했을때 증상 있는 외래 환자의 심혈관 사건을 단독으로 쓸때보다 더 잘 예측했다고 보고함
관상동맥 질환(CAD)이 의심되는 환자에게 CCTA와 CSCT를 따로 두 번씩 찍는것이 관행인데, 본 연구의 자동화 알고리즘은 방사선 노출을 줄이는데 도움이 됨
CSCT 없이도 CCTA만으로 CAC 점수를 안정적으로 추출할 수 있다면, 협착성 CAD 환자에게서 방사선 노출이 줄어들 수 있으며, 환자당 평균 0.5mSv 정도의 방사선 감소가 예상
본 연구의 완전 자동화 앍리즘은 방사선사들의 수작업 기반 CAC 점수 계산 업무를 줄임
* 시간 절약 + 인력 절약 + 환자 부담 감소
한계점1. underestimation
모델로 추출한 volume, Agatston score의 절대값이 기준값보다 유의미하게 작았다
이 현상은 CCTA, CAC가 과소평가된다는 기존 연구들과 일치
조영제와 석회화 플라크가 유사한 감쇠도를 가질때 발생하는 masking effect때문에 과소평가 된다고 보임
하지만, Agatston score 계산 시에는 이효과를 보정한 것으로 보이며, volume score보다 차이가 작거나 유의하지 않았음
또한, 심혈관 사건 예측이라는 임상적 관점에서도 매우 중유한 '위험군 분류 성능'은 본 모델이 우수하게 수행했음
한계점2. 단일기관 데이터
외부 검증은 수행되었지만 본 연구는 단일 기관에서 시행한 것
기관마다 조영제 및 영상 획득 프로토콜에 차이가 있기 때문에, 루멘 감쇠도에 차이가 생길 수 있음
결론적으로, 본 딥러닝 기반 완전 자동화 정량화 앍리즘은 조영제를 사용하는 CCTA에서 추가 방사선 노출 없이 관상동맥 석회화를 효율적으로 추출학, Agatston score의 위험군 분류를 안정적으로 수행

