논문정보
A comparative analysis of deep learning-based location-adaptive threshold method software against other commercially available software
논문정리
1. Abstract
CCTA(coronary computed tomography angiography) 이미지를 이용해서 관상동맥(coronary artery)를 자동으로 세그멘테이션하면, CAD(coronary artery diesease) 관련 분석을 더 쉽게 할 수 있다.
루멘(lumen)이나 플라크(plaque) 부위를 정확하게 중요하는 것이 중요함!
CCTA
관상동맥 CT 혈관조영술
심장의 관상동맥을 비침습적으로 촬영하여, 혈관이 좁아졌는지(협착), 막혔는지 (폐쇄) 등을 평가하는 검사
조영제를 정맥에 주입한 뒤 CT로 촬영
Lumen
혈관 안쪽 공간, 피가 실제로 흐르는 통로
루멘의 크기가 좁아졌는지를 보고 CAD를 판단
(e.g., 정상보다 좁아져있으면 협착)
Plaque
혈관 벽 안쪽에 쌓인 지방, 콜레스테롤, 석회질 같은 침착물
시간이 지나면서 혈관을 좁게 만들고, 때로는 터져서 심근경색을 유발
(e.g., 어디에 있고, 얼마나 두꺼우며, 단단한지-석회화, 말랑한지-비석회화 등을 봄)
● 루멘 : 현재 피가 잘 흐르고 있는지
● 플라크 : 앞으로 막힐 위험이 있는지
이 연구는 딥러닝 기반의 location-adaptive 임계값 방법(DL-LATM, deel learning-based location-adaptive threshold method)을 사용한 소프트웨어 플랫폼이 기존의 상용 소프트웨어들과 비교했을 때, 관상동맥 분할을 얼마나 잘 수행하는지 CCTA 영상을 이용해 분석
환자 19명에게서 26개 혈관 구간에 대한 IVUS(intravascular ultrasound) 데이터를 얻어, 각 소프트웨어의 성능을 평가하기 위한 기준으로 사용
각 소프트웨어가 측정한 루멘, 플라크 수치를 IVUS 데이터와 비교하여 통계분석 (PCC, ICC, Bland-Altman plot) 수행
DL-LATM기반 소프트웨어는 루멘 부피나 면적을 측정할때 오차가 거의 0에 가까웠고 PCC, ICC 값도 높았음
- 루멘 부피 평균 차이 -9.1mm³, 95% 신뢰구간 -18.6~0.4mm³,
- 면적 평균 차이 -0.72mm²
IVUS
혈관 안에 초음파 기기를 넣어서 혈관 단면을 고해상도로 촬영하는 검사
기기를 혈관에 삽입해야 해서 침습적 검사
매우 정밀해서 정답처럼 사용
PCC (Pearson Correlation Coefficient)
피어슨 상관계수
두 수치 간의 선형적인 관계가 얼마나 강한지를 보여줌
값 간 패턴 유사성
ICC (Intraclass Correlation Coefficient)
군내 상관계수
같은 대상에 대해 여러 측정값이 얼마나 일치하는지를 평가함
값 간 정확한 일치
협착 부위의 루멘과 플라크 면적도 분석함
여기서도 DL-LATM 기반이 루멘과 플라크에서 모두 오차가 가장 적었고 PCC가 훨씬 높았음 ($p<0.001$)
- 루멘 면적 평균 차이 -0.07 mm², 95% 신뢰구간 -0.16~0.02 mm²
- 플라크 면적 평균 차이 1.70mm², 95% 신뢰구간 1.37~2.03 mm²
즉, DL-LTAM 기반 소프트웨어가 관상동맥 질환 진단 보조 시스템으로서 잠재력을 보여줌
2. Introduction
관상동맥 질환(CAD)은 전 세계적으로 사망 원인 1위로 심혈관계와 관련된 질환들을 유발
CCTA 영상으로 관상동맥을 자동으로 세그멘테이션 하고, 이를 통해 CAD와 관련된 다양한 분석 수행
관상동맥을 세그멘테이션하는 여러 방법들이 있긴 한데, 정확환 3D 혈관 모델을 만들기 위해선 여전히 수동 세그멘테이션 작업이 필요하며, 이 경우 관찰자 간/내 편차가 발생
따라서, 최근에는 CCTA 연구들이 딥러닝 알고리즘을 활용하여, 특히 관상동맥 세그멘테이션에 초점을 맞추고 있음
intra-observer variability
같은 사람이 반복 측정해도 오차가 생기는 경우
inter-observer variability
사람마다 측정 결과가 달라지는 경우
혈관이 좁아진(협착된) 부위에서 혈류가 감소하기 때문에 루멘의 협착정도는 CAD 진단에 중요한 요소임
+혈관 내 플라크를 구성하는 성분들(e.g., 지질과 칼슘)도 중요
따라서, 협착 부위에서의 루멘이나 플라크 부피를 정확히 측정하려면 자동 세그멘테이션 기술을 이용한 정밀탐지가 선행되어야 함
루멘의 협착정도
▶ 혈류 흐름과 관련
▶ 혈류가 줄어들면 심장 근육에 산소 공급이 부족해져 협심증이나 심근경색으로 이어질 수 있음
플라크의 성분
▶단순히 크기뿐 아니라 성질까지 반영하는 지표
▶지질이 많은 플라크는 잘 터져서 심근경색 위험이 큼
이전 연구들은 LATM이 협착 부위에서의 관상동맥 세그멘테이션 문제를 해결할 수 있다는 것을 보여주었고
이후 딥러닝 기술과 LATM을 결합한 DL-LATM이 개발되었음
DL-LATM 기반 소프트웨어의 루멘 및 플라크 분할 성능은 기존 상용 소프트웨어들과 비교평가됨
- 소프트웨어간 성능은, IVUS 데이터를 기준으로 사용하여 비교
이 연구의 목적은 DL-LATM의 전체적인 분할 성능, 특히 협착부위에서의 성능을 평가하여 CAD 진단을 돕는 보조 시스템으로서의 가능성을 확인하는 것
2. Materials and methods
2.1 Subjects
22명의 환자에게서 30개의 관상동맥 구간을 추출
CAD가 의심되거나 진단받은 환자들은 2009.03.01~2010.06.31일 내 서울대학교병원에서 CCTA와 IVUS를 포함한 침습적 관상동맥 조영술을 받음
● 제외기준
- 움직임(motion artifact)로 인해 CCTA 영상 품질이 나쁜 경우 (4개)
- 소프트웨어 분할 실패
● 분할 실패 기준
- 파일 로드 실패
- 기준 데이터(IVUS)와 측정값 차이가 매우 큰 경우
기준 데이터와 측정값 차이가 크면, 분할 성능 평가에 편향이 생길 수 있다.
최종적으로 19명의 환자에게서 추출한 26개의 관상동맥 구간이 연구에 포함됨
(평균 연령: 64.6세, 여성 비율: 15.3%)
2.2 CCTA image acquisition and reconstruction
● 사용된 CT 장비 종류 및 인원
- Dual-source Ct (17)
- 16-slice Ct (8)
- 256-slice CT (1)
- 기기 : Simens SOMATON Definition, Sensation 16, Philips iCT)
● 조영제 투여
- 팔꿈지 정맥(antecubital vein)에 경로 확보
- Iopromide (Ultravist 370) 70-90 ml 주입
- 후속 주입 (생리식염수 8: 조영제 2 비율의 혼합액 50ml를 4ml/s 속도로 주입, 장비는 듀얼 파워 인젝터)
● CT 스캔 시작 조건
- 조영제의 신호 강도를 상행 대동맥(mid ascending aorta)에서 실시간 모니터링
- 기준선보다 150HU 이상 신호가 상승한 후 8초 후 촬영 시작
● 스캔 파라미터
- Collimation: 32 × 0.6 mm / 16 × 0.75 mm / 128 × 0.625 mm
- tube voltage: 100 kVp 또는 120 kVp → 환자의 체형(body habitus)에 따라 조정
- Tube current: 140-620 mA
- Rotation time: 270-370ms
● 재구성 파라미터
- 재구성 방식: Mono-segment reconstruction algorithm, ECG 신호에 맞춘 retrospective gating 방식
- Slice thickness: 0.8-1mm
- Increments: 0.5-0.7mm
- Kernel: 중간 강도의 소프트 커널
영상 재구성
CT 스캐너가 촬영한 원시 데이터를 가지고, 우리가 실제로 보는 단면이미지를 만들어내는 과정
● 촬영 시점
- 심장 박동 중 중간 이완기(mid-diastolic phase)에 촬영
심장 움직임이 가장 적은 시점, 모션 없는 데이터 확보
2.3 IVUS imaging protocal and analysis
● 장비 및 기본 정보
- 사용한 카테터: 40MHz, 2.9F ( Boston Scientific Scimed)
- 해상도
- 축 방향(axial): ±80 μm
- 횡 방향(lateral): ±200 μm
카테터
몸속에 삽입해서 액체를 넣거나 빼기 위한 가느다란 튜브
● 검사 절차
- 검사 전 관상동맥에 니트로글리세린 투여 ➡️ 혈관 확장
- IVUS 촬영 방식
- 목표 혈관 구간 전체에 대해 촬영 수행
- 자동 모터를 이용한 pullback 방식 사용 (속도: 0.5mm/s , 프레임속도: 30장/초)
● 영상 분석
- 담당자: 15년 경력의 심장 전문의, EchoPlaque 소프트웨어 사용
- 루멘 면적 측정
- 루멘-내막(lumen-intima) 경계선과 외부 탄성막(external elastic membrane)을 각 단면마다 수동으로 그려서 측정
- 플라크 부피 계산
- simpson's rule을 사용하여 여러 단면 면적을 이용해 부피 계산
● CT - IVUS 매칭
- IVUS의 위치 기준: 혈관 분지(branch)를 기준점으로 삼아 위치 기록
- CCTA 3D 이미지에서 일부 부위 표시
- 병변 길이와 방향 포함한 위치 정보 제공
요약
IVUS는 고해상도 초음파 카테터를 사용해 목표 혈관 구간 전체를 자동으로 이동하며 단면 이미지를 얻고, 전문의가 직접 루멘과 혈관벽 경계를 따라가며 면적을 측정하고, 이를 통해 플라크 부피를 정밀하게 계산한다. 그 위치 정보를 CCTA 영상과 매칭하기 위해, 혈관 분지나 병변 길이 등을 기록해 정합 근거로 사용한다.
2.4 Measurement of lumen or plaque parameters for three software platforms
모든 소프트웨어는 수동 수정 없이 완전 자동 방식으로 관상동맥을 세그멘테이션 함
루멘 및 플라크 영역을 단면마다 자동 측정
● 사용한 소프트웨어
- AutoSeg (AI Medic)
- syngo.via (Siemens)
- IntelliSpace Portal (Philips)
IVUS에서 제공된 위치 정보를 바탕으로 CCTA 상에서 동일 혈관 구간 위치를 매칭
이후 소프트웨어별로 단면마다 루멘/플라크 면적 측정

(a) 3D 심장 CT 이미지 + 분석대상 혈관 표시
Left anterial descending (LAD, 심장왼쪽에서 시작해서 심장 앞쪽을 아래로 내려가는 혈관) artery 중 just distal LAD 부위(LAD의 바로 아래쪽 구간), 15mm가 분석 대상
이 부위가 IVUS와 CCTA 모두에서 분석된 대상 혈관
(b) IVUS 단면 이미지
혈관을 안에서 초음파로 찍은 단면
노란 선: 루멘
빨간 선: 플라크 포함한 경계
(c-d) Longitudinal and curved planar reformation(cpr) 이미지
이걸 이용해서 3D 구조를 재구성하거나 부피 계산이 가능함
단면들이 시간순서로 쭉 나열됨
그러니까, 혈관이 굽어있는데, 이걸 평평하게 펴서 길이방향을 표현한 것
(c) IVUS로 한 혈관을 0.5mm/s 속도로 스캔한 결과
(d) CCTA를 소프트웨어1(autoseg)를 이용해서
(e-g) 각 소프트웨어가 세그멘테이션한 단면 영상들
안쪽선과 바깥쪽선은 각각 루멘 경계와 혈관 외벽 경계
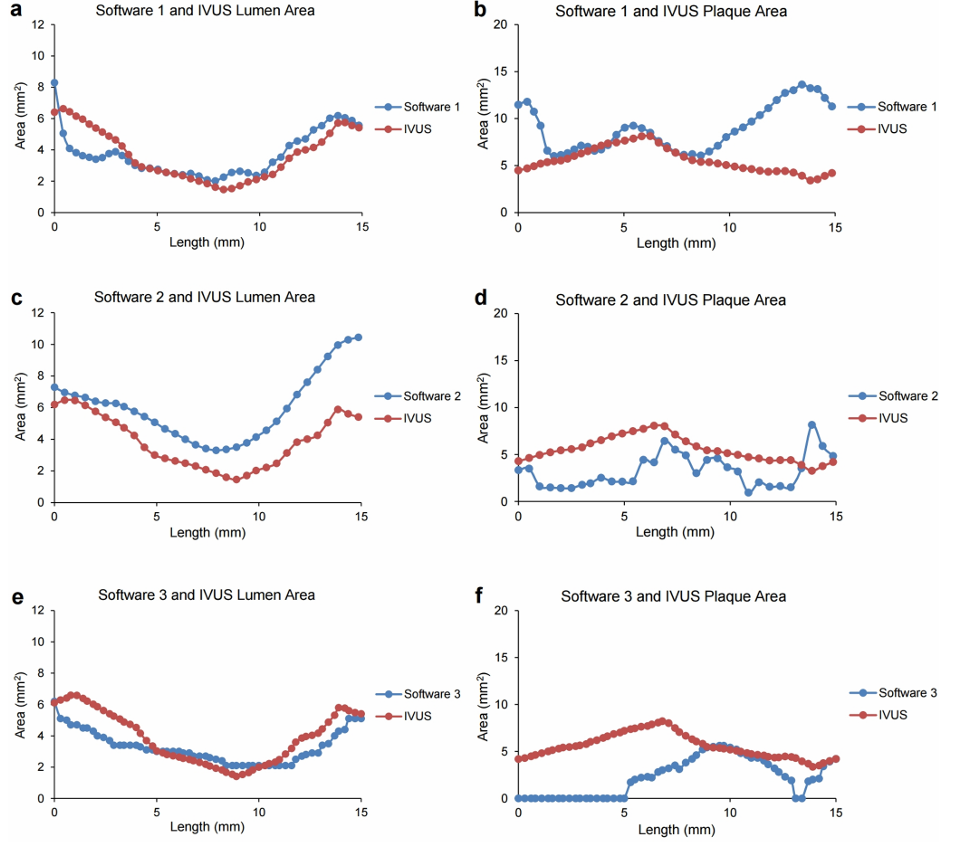
IVUS 단면 데이터는 0.001mm 간격, 소프트웨어들은 0.2~0.5mm 간격으로 단면을 구분하여 간격이 서로 다름
▶ IVUS 데이터를 소프트웨어 간격에 맞게 보정하였음
루멘/플라크 부피 = 단면 면적들의 합 * 소프트웨어 간격값
이렇게 CCTA 기반 부피값을, IVUS에서 측정된 정답부피와 비교하여 정확도를 평가하였음
2.5 Deep learing-based location-adaptive threshold method for calculating lumen or plaque area
루멘과 플라크의 면적은 AI medic에서 개발한 전용 소프트웨어 Autoseg-H v1.05를 사용해 측정
이 논문에서 사용된 CCTA 영상들은 DL-LATM 모델을 개발할 때 학습에 사용되지 않음
▶ 학습 데이터와 평가 데이터 분리
소프트웨어는 Ai와 수치 해석 기법을 혼합해서 centerline과 딥러닝 기반 보정계수를 자동으로 찾고 세그멘테이션
● Centerline
- V-net(컨볼루션 신경망)을 사용하여 관상동맥의 3D 모델 생성함
- 231,219장의 수동 분할된 관상동맥 CT 이미지로 학습됨
● 보정 계수
대동맥을 Deeplab v3+로 세그멘테이션 하여 생성
103,076장 수동 라벨된 대동맥 CT 이미질 학습
이후 XGBoost(스케일 문제를 해결)로 영상 스케일 기반 보정값 추출
Centerline을 따라 자른 단면에서, 고정된 HU 임계값을 사용하는 대신, DL-LATM 방법을 사용하여 루멘과 혈관 외벽 경계를 자동으로 분리
경게를 찾을때 인접 픽셀간의 CT 강도 (HU) 차이가 중요함!
루멘에서 외벽 방향으로 갈수록 가장 강하게 HU 값이 변화하는 지점을 찾아서 루멘 경계 및 혈관 외벽 경계를 판별
루멘 경계를 결정하기 위해, HU 기준으로 상하한값을 정함
Calcification(석회화)를 제외하기 위해, 루멘 상한 값은 inner point의 145%로 설정
혈관 외벽 경계의 하한값은 inner point의 50%로 설정
DL-LATM은 기존 LATM 방법을 기반으로 한 딥러닝 알고리즘
LATM은 FWHM을 기반으로 설계되어서 하한HU 임계값을 inner point의 50%로 설정
플라크 영역은 전체 혈관 외벽에서 루멘을 뺀 영역으로 정의
inner point와 calibration factor간 HU 차이가 너무 크면(inner point>calibration factor*1.45 or <0.5), 임계값을 inner point 대신 calibration factor 기준으로 경계를 설정함
원래는 inner point를 기준으로 해서 상하한값 범위로 HU 변화가 급격한 위치를 경계로 잡음
그런데 inner point 값이 비정상적이면 임계값도 틀어져서 경계 인식 오류 발생
▶innter point가 calibration factor와 너무 다르면 임계값 계산을 calibartion factor로 대체
* calibration factor의 역할
정상적인 루멘 HU가 대략 어느 수준일지를 미리 추정해주는 기준값
DL-LATM은 각 단면에서 루멘 경계를 적응적으로 계산하는데, calibration factor을 이용하여 기존 LATM이 협착 부위에서 루멘을 과대평가하던 문제를 극복할 수 있었음
세그멘테이션된 각 단면들을 조합하여, 3D 관상동맥 모델 생성
기존 LATM 알고리즘에서 루멘을 overestimate하게 된 이유
협착 부위가 어둡기 때문!
inner point값이 작아지고, 그 작은값 기준으로 하한값을 잡음 => 혈관벽을 넘어서도 루멘이라고 보는것
e.g., 정상값이 300이면 하한값은 150이 되는데, 협착 부위에서 180이면 하한값이 90이 됨
2.6 Subgroup lumen or plaque area analysis in the stenotic region
IVUS 데이터에서 측정된 plaque burden값을 이용해 루멘이나 플라크 면적에 대한 subgroup 분석을 수행함
* Plaque burden
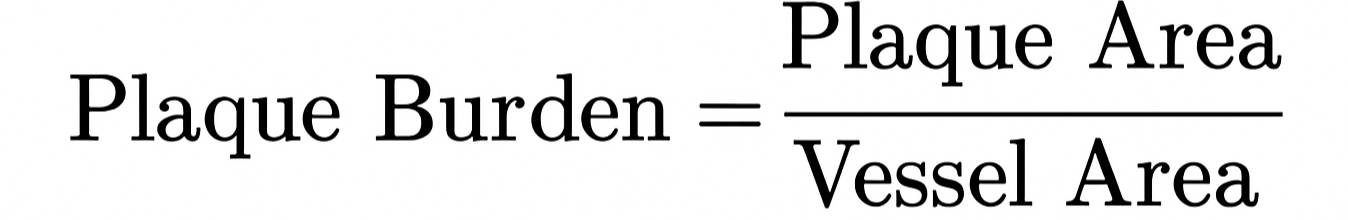
(혈관 전체 면적 중 플라크가 차지하는 비율)
관상동맥 병변 (coronary lesions)은 보통 루멘은 좁고, 플라크가 넓게 둘러싼 구조를 보임
High plaque burden
Plaque burden이 0.6보다 큰 협착 구간 (stenosis region)을 대상으로 루멘과 플라크 면적을 3개 소프트웨어로 측정 후 IVUS 값과 비교
2.7 Statistical analysis
일치도 평가를 위해 Bland-Altman plot을 사용
일치 범위(limits of agreement)는 측정값 차이의 평균 ± 1.96 × 표준편차(SD)로 정의
이 외에도, PCC와 ICC로 각 소프트웨어의 IVUS 기준 대비 신뢰도를 평가함
ICC 계산은 2-way random effects model, single measurement, absolute agreement 기준으로 수행
PCC를 비교하기 위해 독립된 집단 간 Fisher's r-to z 변환법을 사용하였음
$p$ ≤ 0.05를 통계적으로 유의미한 차이로 간주
3. Results
3.1 Comparison of lumen or plaque volume for three different software platforms
각 소프트웨어의 루멘과 플라크 세그멘테이션 정확도를 분석하기 위해 각 target segment에 대해 소프트웨어가 계산한 루멘, 플라크의 부피를 IVUS 기준값과 비교
이에 대한 PCC, ICC 분석 결과는 IVUS 데이터를 정답으로 하여 표1에 제시

루멘 부피에 대한 PCC는 세 소프트웨어 모두 유사
플라크 부피에 대한 PCC는 소프트웨어1이 가장 높음
ICC는 모두 소프트웨어 1이 가장 높음
각 부피에 대한 Bland-Altman plot은 그림 3에 제시

루멘 부피에서, 소프트웨어 1이 평균 차이가 0에 가장 가까운 bias를 보임
(mean difference = -9.1 mm³ , SD = 24.2 mm³ , 95% confidence interval [CI] = -18.6 to 0.4 mm³)
플라크 부피에서는 소프트웨어2의 bias가 가장 0에 가까웠는데
(mean difference = -8.5 mm³ , SD = 70.3 mm³ , 95% CI = -39.3 to 22.3 mm³)
가장 낮은 변동성은 소프트웨어 1이 보였음
(mean difference = 33.8 mm³ , SD = 49.1 mm³ , 95% CI = 14.6 to 53.0 mm³)
3.2 Comparison of lumen or plaque area for three different software platforms
루멘과 플라크 면적에 대한 PCC, ICC 통계 분석 결과는 표2에, Bland-Altman plot은 그림4에 있음
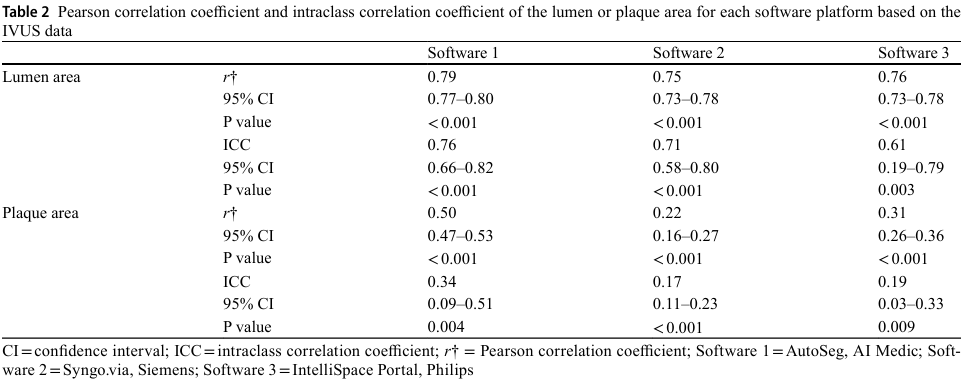
소프트웨어 1이 루멘, 플라크 면적에서 PCC, ICC가 모두 높았음
루멘과 플라크 면적에 대한 소프트웨어 1의 ICC 값은 다른 소프트웨어보다 통계적으로 유의미하게 높았다 (각각 p-value가 0.005, <0.001)

루멘 면적에서는 소프트웨어 1이 bias가 0에 가장 가까움
(mean difference = -0.72 mm², SD = 1.71 mm², 95% CI = -0.80 to -0.64 mm²)
플라크 면적에서는 software 2가 bias가 0에 가장 가까운데
(mean difference = -0.90 mm², SD = 4.40 mm², 95% CI = -1.17 to -0.63 mm²)
SD는 소프트웨어1에서 가장 낮음
(mean difference = 2.76 mm², SD = 3.88 mm², 95% CI = 2.58 to 2.94 mm²)
즉, 루멘 면적/부피에서는 소프트웨어 1이 PCC, ICC, bias, SD 모두 우수함
플라크 면적/부피에서는 소프트웨어 2가 bias는 가장 0에 가까웠지만 SD값이 커서 결과가 불안정하며,
소프트웨어 1은 bias는 약간 높지만, SD가 작아서 더 안정적이고 일관된 결과를 보임
3.3 Subgroup lumen or plaque area analysis in the stenotic region
임상적으로는 관상동맥 병변을 정확하게 세그멘테이션 하는 것이 중요함
plaque burden이 0.6 이상인 협착 부위를 대상으로, 각 소프트웨어별 루멘 및 플라크 면적의 하위 그룹을 분석한 후 IVUS 데이터와 비교함
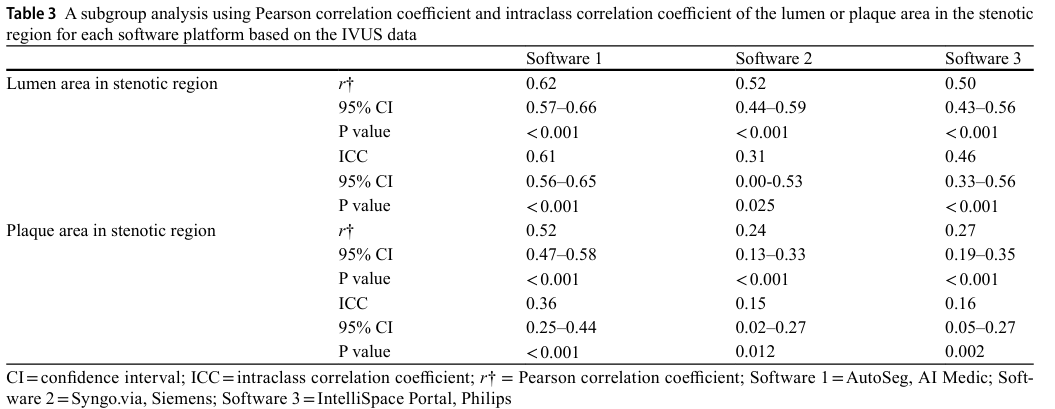
소프트웨어 1이 루멘과 플라크 면적 모두에서 가장 높은 PCC, ICC를 기록
협착 부위에서의 루멘 및 플라크 면적에 대한 소프트웨어 1의 ICC 값은 다른 소프트웨어보다 통계적으로 유의미하게 높았음 (p<0.001)

협착 부위에서 소프트웨어 1이
- 루멘 면적의 평균 차이가 -0.07mm²로 0에 가장 가까움
- 플라크 면적에 대해서도 평균 차이가 1.70mm²로 가장 근접
- 표준편차 및 신뢰구간
- 루멘 SD = 1.36, CI = -0.16 ~ 0.02
- 플라크 SD = 4.61, CI = 1.37 ~ 2.03
4. Discussion
본 연구는 딥러닝 기반 DL-LATM 방식이 협착 부위의 루멘,플라크를 얼마나 정확히 세그멘테이션할 수 있는지를, IVUS 데이터를 기준으로 평가하여 기존 상용 소프트웨어들과 비교
관상동맥 세그멘테이션 소프트웨어의 서브그룹 분석 결과
- 소프트웨어1이 루멘을 탐지할때, 가장 높은 PCC와 ICC, 가장 작은 평균 차이 (bias ≈ 0)를 보임, 플라크 영역에서도!
(협착 구간에서, IVUS 데이터를 기준으로) - 협착 부위에서 루멘, 플라크 면적을 탐지할 때, 소프트웨어 1의 ICC가 다른 것들보다 유의미하게 높았음
결론! 제안된 DL-LATM 방식은, 기존 LATM이 협착 부위에서 루멘 경계를 overestimate 하던 한계를 극복
모든 소프트웨어에서, 플라크 보다 루멘 세그멘테이션 성능이 더 우수함
why? 혈관 외벽을 감지하는 것이 루멘을 감지하는 거보다 더 어려움
소프트웨어2는 심방이나 정맥 근처 일부 위치에서 플라크 영역을 과도하게 크게 측정
반대로, 소프트웨어 3은 협착이 없는 부위에서 플라크 면적을 비정상적으로 작게 측정
소프트웨어 1은 협착이 없는 부위에서 플라크 면적을 과대평가
혈관 외벽(outer vessel boundary)를 감지하려면, 해당 지점의 HU 감쇠도가
- 주변 픽셀 보다 큰 변화(gradient)를 보이며
- inner point HU의 50% 미만이어야 함
이런 특성은 플라크가 많은 협착 부위에서는 명확히 잘 나타남
but, non-stenotic region에서는 이 기준이 플라크 면적의 과대평가로 이어질 수 있음
플라크가 많을 때
경계가 뚜렷하고 HU 값이 급격히 변함
플라크가 적을 때
실제 경계보다 다른 HU 급감 지점이 더 눈에 띌 수 있음
그런데 플라크 부담이 높은 구간에서의 세그멘테이션 중요성을 고려하면 소프트웨어 1은 협착 부위에서 플라크 면적에 대해 bias가 가장 낮았음
연구에 몇 가지 제한점이 있음
1. 적은 샘플수 (n=26)
이를 보완하기 위해, 충분한 수의 단면에서 루멘과 플라크 면적을 분석하여 더 많은 정보를 추출
2. 소프트웨어간 불일치
IVUS 데이터의 단면간격은 0.001mm, 소프트웨어들은 0.2~0.5mm
▶ IVUS의 단면 간격을 각 소프트웨어에 맞게 적응적으로 조정
근데 IVUS의 시작점과 단면위치가 CT이미지와 정확히 일치하지 않을 수 있어서, 간격을 조정해도 전체 상관계수를 떨어뜨릴 수 있음
전체 상관계수에서는 영향을 주지만, 소프트웨어간 세그멘테이션 성능 비교에는 영향이 없다
이 연구는 협착 부위에서의 세그멘테이션 성능에 집중하여 소프트웨어 비교
향후에는
- 협착률 추정
- 플라크 유형 분류 비교
- CT-FFR 계산을 통한 CAD 평가로 확장 가능
특히, DL-LATM으로 생성한 3D 모델은 CT-FFR 계산용 입력으로 활용 가능
- 비침습적 CAD 진단에 기여 가능
5. Conclusions
DL-LATM이 적용된 소프트웨어 플랫폼이 기존 상용 소프트웨어와 비교하여 협착 부위에서 루멘과 플라크 면적을 탐지하는데 있어 신뢰할만한 성능을 보임
이 소프트웨어를 CAD 진단을 위한 보조 시스템으로 제안
The Bland-Altman plots for the lumen or plaque area in the stenotic region

